Introducción
Margaret H. Hastings, y col. Intrinsic and Extrinsic Contributors to the Cardiac Benefits of Exercise,JACC: Basic to Translational Science,2023,ISSN 2452-302X, https://doi.org/10.1016/j.jacbts.2023.07.011. (https://www.sciencedirect.com/science/article/pii/S2452302X23002942)
La importancia del ejercicio en la prevención de las enfermedades cardiovasculares ha sido reconocida durante mucho tiempo.
Las pautas de actividad física establecidas por el American College of Cardiology y la American Heart Association sugieren entrenamiento de ejercicio cardiorrespiratorio de intensidad moderada durante al menos 30 minutos al día, 5 días a la semana para adultos sanos.
Además de reducir el riesgo de enfermedades cardiovasculares, el ejercicio mejora la capacidad funcional y la calidad de vida en poblaciones con enfermedades cardiovasculares, como en insuficiencia cardíaca, y puede mejorar los resultados clínicos, aunque esto último ha sido difícil de establecer de manera concluyente.
Los cambios inducidos por el ejercicio en el crecimiento, la proliferación y la función de los cardiomiocitos son fundamentales para muchos de los efectos cardíacos del ejercicio.
Sin embargo, hay un creciente reconocimiento de roles clave de las líneas celulares no cardiomiocíticas en el corazón, incluidas las fibras y las células vasculares, la microcirculación coronaria y los sistemas linfáticos.
Además, las vías y procesos que ocurren principalmente fuera del corazón son cada vez más apreciados como contribuyentes a las enfermedades, así como a los beneficios del ejercicio.

El Músculo, Ejercicio y Salud Cardiometabólica
Llévate esta formación y coloquio, El Músculo, Ejercicio y Salud Cardiometabólica, con el Dr. José López Chicharro
Efectos Cardiacos Inrínsecos
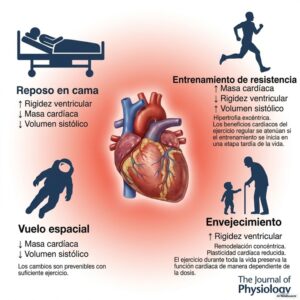
Los cardiomiocitos son responsables de algunos de los fenotipos más destacados del ejercicio, incluyendo el crecimiento cardíaco (hipertrofia) y las alteraciones en la función.
Crecimiento y proliferación de los cardiomiocitos en la hipertrofia cardiaca fisiológica.
Los cardiomiocitos representan solo alrededor del 30% al 40% de las células del corazón, pero son responsables de alrededor del 70% al 85% de su volumen, y el entrenamiento de resistencia aeróbica conduce a un agrandamiento cardíaco (hipertrofia), debido principalmente a un aumento en el tamaño de los cardiomiocitos.
A pesar de parecer similar superficialmente al crecimiento cardíaco patológico que acompaña a las enfermedades cardiovasculares y a menudo precede a la insuficiencia cardíaca, la hipertrofia fisiológica inducida por el ejercicio difiere en que es reversible y, en lugar de disfunción, está asociada con protección contra el estrés patológico.
El ejercicio también aumenta proporcionalmente la longitud y el ancho de los cardiomiocitos, mientras que la hipertrofia patológica aumenta desproporcionadamente la longitud de los cardiomiocitos.
Es importante destacar que el entrenamiento aeróbico protege contra la hipertrofia patológica en modelos de ratones y, en algunos casos, revierte este proceso, lo que respalda las diferencias fundamentales y la tensión dinámica entre ambos.
La cardiomiogénesis puede contribuir a los beneficios clínicos del ejercicio en parte al contrarrestar la pérdida de cardiomiocitos que se cree que contribuye a la insuficiencia cardíaca en múltiples situaciones. Sin embargo, será importante evaluar rigurosamente las implicaciones funcionales de la cardiomiogénesis inducida por el ejercicio dada la baja cantidad absoluta de cardiomiocitos formados.
Modificaciones en la función de los cardiomiocitos.
Algunos de los beneficios del ejercicio reflejan cambios en la función de los cardiomiocitos.
El entrenamiento aumenta la función sistólica y diastólica del corazón tanto en la salud como en la enfermedad, con importantes implicaciones para la calidad de vida. Aunque la modificación de la precarga y la postcarga contribuyen a la mejora de la función cardíaca, también contribuyen los cambios en las propiedades cronotrópicas, inotrópicas y lusitrópicas del corazón.
Estudios en animales han confirmado que el entrenamiento aeróbico puede aumentar la fracción de acortamiento de los cardiomiocitos hasta en un 40% a 50%, las tasas de contracción y relajación hasta en un 20% a 40%, y la potencia máxima de salida hasta en un 60%. Estos efectos dependen de la intensidad del ejercicio y retroceden rápidamente con el desentrenamiento.
Efectos del ejercicio en la función de los cardiomiocitos en enfermedades y envejecimiento.
Las vías endógenas reguladas por el ejercicio pueden proporcionar objetivos terapéuticos, no solo para las enfermedades cardíacas, sino también para el deterioro de la función cardíaca que ocurre en el envejecimiento normal.
El ejercicio puede revertir la rigidez del ventrículo izquierdo en el envejecimiento sedentario y en individuos de mediana edad con hipertrofia ventricular izquierda en riesgo de insuficiencia cardíaca.

CARDIOPATÍA ISQUÉMICA, valoración de riesgo y prescripción de Ejercicio Físico
Llévate esta formación, CARDIOPATÍA ISQUÉMICA, valoración de riesgo y prescripción de Ejercicio Físico, junto a +50 cursos de fisiología del ejercicio (fuerza, nutrición deportiva, entrenamiento, rendimiento, salud y deporte, etc...), supervisados por el Dr. Jose López Chicharro
Fibrosis Cardíaca.
Mientras que la hipertrofia patológica y el deterioro cardíaco relacionado con la edad se asocian con la fibrosis intersticial, la hipertrofia fisiológica generalmente no lo hace.
Los animales entrenados con ejercicio desarrollan menos fibrosis que los animales de control sedentarios en respuesta a lesiones cardíacas o estrés patológico, incluyendo hipertensión, sobrecarga de presión y lesiones isquémicas, entre otros.
Aunque los roles de los fibroblastos son multifacéticos e incluyen importantes funciones estructurales, mecánicas y de reparación, estas observaciones sugieren que, además de los efectos favorables en los cardiomiocitos discutidos anteriormente, el ejercicio puede reducir el remodelado cardíaco adverso en parte al limitar la fibrosis.
Posibles beneficios y riesgos de reducir la fibrosis en enfermedades y envejecimiento.
Aunque la fibrosis es una característica distintiva del remodelado cardíaco adverso en los ancianos, sigue siendo un desafío definir la contribución de la fibrosis en sí misma a estas condiciones.
La fibrosis excesiva puede deteriorar la función sistólica y diastólica del corazón, así como provocar arritmias, pero los fibroblastos también desempeñan roles importantes en la homeostasis, generando la matriz extracelular que sirve como andamio del corazón, contribuyendo a la respuesta del corazón al estrés mecánico, reemplazando los cardiomiocitos perdidos y mediando la formación de cicatrices después de una lesión.
Por lo tanto, los beneficios y riesgos de dirigirse a la fibrosis probablemente varían en diferentes contextos, con preocupaciones sobre posibles rupturas, especialmente después de un infarto.
Los fibroblastos no son tan críticos como se pensaba generalmente, o el sistema puede compensar una pérdida considerable de fibroblastos.
Cabe destacar que se ha informado de fibrosis miocárdica focal en atletas de resistencia aeróbica de larga duración en algunos, pero no en todos los estudios, lo que sugiere que el ejercicio puede promover la fibrosis en algunas condiciones, aunque la causalidad es incierta dada la presencia de factores de confusión inherentes en los estudios observacionales.
Vasculatura Cardíaca.
Clínicamente, se presta considerable atención a los vasos epicárdicos debido a su papel en los síndromes coronarios agudos, así como en la isquemia y el infarto de miocardio.
Si bien el ejercicio tiene efectos importantes a este nivel, cada vez se reconoce más la importancia de otros componentes vasculares, en particular la microcirculación coronaria y los linfáticos cardíacos.
Microcirculación coronaria.
La microcirculación coronaria comprende una red ininterrumpida de vasos sanguíneos cardíacos con diámetros que disminuyen desde prearteriolas (500-100 µm de diámetro) hasta arteriolas (<100 µm de diámetro) y capilares.
Esta microvasculatura regula la perfusión del miocardio para igualar el suministro de sangre con el consumo de oxígeno.
En escalas de tiempo cortas, como durante el ejercicio agudo, los ajustes rápidos en el flujo sanguíneo se logran principalmente mediante cambios en el diámetro de las prearteriolas y las arteriolas.
Sin embargo, la microvasculatura coronaria también experimenta adaptaciones estructurales y funcionales a largo plazo debido al ejercicio crónico.
El entrenamiento de ejercicio mejora tanto la constricción miogénica inducida por la presión y dependiente del músculo liso como la dilatación dependiente del endotelio y del cizallamiento en las arteriolas coronarias.
El diámetro y la densidad de las arteriolas, así como la superficie y la permeabilidad capilar, aumentan.
El entrenamiento disminuye el módulo elástico y aumenta el grosor de la pared, la tensión de la pared y la distensibilidad en las arteriolas coronarias de ratas.
A diferencia de la hipertrofia patológica, en la que el crecimiento del músculo puede superar la angiogénesis, lo que probablemente contribuye a la insuficiencia cardíaca, el entrenamiento con ejercicio induce angiogénesis capilar proporcional al crecimiento cardíaco. El ejercicio también puede proteger indirectamente la microcirculación coronaria al mitigar la inflamación, la activación plaquetaria, la disfunción autonómica y las fuerzas hemodinámicas.
Adaptaciones de la microcirculación coronaria inducidas por el ejercicio en el envejecimiento y las enfermedades.
El ejercicio regular beneficia a los pacientes con enfermedades que involucran la disfunción de la microcirculación coronaria, incluyendo la insuficiencia cardíaca y la enfermedad de las arterias coronarias, entre otras.
Respaldando un papel de los cambios en la microvasculatura en los beneficios clínicos del ejercicio, el entrenamiento de intervalos aeróbicos de 12 semanas aumentó la reserva de flujo coronario en pacientes con enfermedad de las arterias coronarias.
El envejecimiento también se asocia con disfunción de la microvasculatura coronaria, y los cambios en la microvasculatura también pueden contribuir a los beneficios del ejercicio en el envejecimiento. El ejercicio moderado mejoró la función microvascular de las piernas en adultos mayores.
Sistema linfático cardíaco.
Hallazgos recientes sugieren un papel del sistema linfático cardíaco en los beneficios del ejercicio.
Los vasos linfáticos desempeñan funciones esenciales y dinámicas en el mantenimiento de la presión intersticial, el transporte de lípidos y la eliminación de antígenos y células inmunitarias, así como en la adaptación específica de los órganos al microentorno local.
El ejercicio regular mejora la función linfática deteriorada tanto en estudios con animales como en ensayos controlados aleatorios con pacientes humanos.
El papel del sistema linfático cardíaco en los efectos terapéuticos del ejercicio no se ha examinado directamente; sin embargo, se ha reconocido durante mucho tiempo la disfunción del sistema linfático cardíaco en enfermedades y se ha documentado en la hipertensión, la aterosclerosis y la dislipidemia, el infarto de miocardio y la insuficiencia cardíaca.
Además, hay evidencia creciente que respalda el crecimiento y la remodelación del sistema linfático cardíaco como posibles objetivos terapéuticos. Se necesita más trabajo para definir las vías de linfangiogénesis reguladas por el ejercicio y la comunicación con los cardiomiocitos, así como para investigar su posible relevancia terapéutica.
Respuestas y Adaptaciones Cardiorespiratorias al Ejercicio
Llévate esta formación, Respuestas y Adaptaciones Cardiorespiratorias al Ejercicio , junto a +50 cursos de fisiología del ejercicio (fuerza, nutrición deportiva, entrenamiento, rendimiento, salud y deporte, etc...), supervisados por el Dr. Jose López Chicharro
Cambios sistémicos con efectos cardiacos.
Metabolismo.
El entrenamiento físico induce cambios metabólicos sistémicos que reducen los factores de riesgo de enfermedades cardiovasculares, como la obesidad y la diabetes.
En parte, esto puede reflejar cambios en la homeostasis energética, aunque este efecto suele ser modesto.
Es probable que sean más importantes la mejora de la sensibilidad a la insulina y la captación de glucosa por el músculo esquelético y otros tejidos, debido en parte al aumento de la expresión del transportador de glucosa GLUT4 y AMPK, una quinasa clave que regula la captación de glucosa.
Otra adaptación sistémica clave relacionada con las enfermedades metabólicas es la inducción del músculo esquelético de la coactivadora de la transcripción PGC-1a, importante en la biogénesis mitocondrial y el metabolismo oxidativo.
En el miocardio, ya sea un aumento de sustrato o una utilización de energía más eficiente son necesarios para respaldar el aumento del tamaño y la función del miocito en respuesta al entrenamiento físico, especialmente en lo que respecta a SERCA2a y otras bombas iónicas involucradas en la función del miocito, que representan la mayor parte de las necesidades de trifosfato de adenosina del corazón.
El entrenamiento físico estimula en el corazón enzimas moduladoras metabólicas (Akt1, deacetilasas dependientes de NAD(+), SIRT-1 y SIRT-3, eNOS) y el sensor de energía AMPK.
A través de objetivos que incluyen PGC-1a y factores de transcripción, como FoxO1 y FoxO3a, estas vías de señalización interconectadas activan redes de transcripción que aumentan las medidas de la masa y función mitocondrial, mejoran el manejo de ácidos grasos y glucosa cardíacos y protegen contra el estrés oxidativo.
Cambios en el metabolismo mediados por el ejercicio en enfermedades y envejecimiento.
El ejercicio también contrarresta directamente los cambios metabólicos observados en el envejecimiento y en corazones enfermos.
La hipertrofia patológica y el envejecimiento cardíaco están asociados con una capacidad respiratoria mitocondrial disminuida, una disminución de la biogénesis mitocondrial, un cambio en la utilización de sustratos de ácidos grasos a glucosa y una producción excesiva de especies reactivas de oxígeno mitocondrial.
Estos cambios reducen la reserva metabólica. En contraste, la remodelación cardíaca fisiológica no está asociada con un cambio de metabolismo de ácidos grasos a glucólisis y se asocia con un aumento de la biogénesis mitocondrial y mecanismos antioxidantes.
El entrenamiento físico mejora el metabolismo cardíaco en modelos de insuficiencia cardíaca en ratones mediante una metabolización más eficiente de ácidos grasos, la restauración del flujo autofágico y un aumento de la biogénesis mitocondrial, reprogramando fundamentalmente el perfil bioenergético del corazón en falla para mejorar su funcionamiento.
Los beneficios metabólicos cardiacos del ejercicio también se extienden a individuos de edad avanzada, aunque parecen ser mayores en personas jóvenes, y esto se relaciona con cambios en la respuesta metabólica al entrenamiento.
Por ejemplo, la expresión de PGC-1a inducida por el ejercicio en los músculos es menor en personas mayores.
Las vías que modulan la adaptación metabólica cardíaca al ejercicio también son necesarias y/o suficientes para proteger al corazón contra el estrés patológico, las lesiones y el envejecimiento.
El entrenamiento físico también mejora los trastornos metabólicos cardíacos y reduce el aumento relacionado con la edad en la producción de especies reactivas de oxígeno mitocondrial. Estos hallazgos preclínicos señalan a los reguladores metabólicos modulados por el ejercicio como objetivos clínicamente relevantes.
Inflamación y Células Inmunitarias.
Como se mencionó previamente, la inflamación es importante en la patogénesis de muchas enfermedades cardiovasculares y los efectos antiinflamatorios del ejercicio son importantes en sus beneficios cardiovasculares.
Experimentos controlados en humanos y modelos animales demuestran una asociación entre los beneficios del ejercicio y una reducción en los marcadores de inflamación, tanto de manera sistémica como en el corazón, tanto durante el envejecimiento como en una variedad de condiciones patológicas, incluyendo insuficiencia cardíaca, infarto de miocardio y aterosclerosis.
Los beneficios antiinflamatorios sistémicos del ejercicio probablemente se deben en parte a una reducción en la acumulación de grasa visceral, que se asocia con la infiltración de células inmunitarias proinflamatorias. Sin embargo, el ejercicio también parece modular directamente el sistema inmunológico, disminuyendo la capacidad de producción de citoquinas de las células mononucleares de sangre periférica en individuos en riesgo de enfermedad cardiovascular.
La inflamación sistémica aumenta con la edad y la obesidad y, debido al envejecimiento de la población y al aumento de la obesidad, representa un problema creciente.
Comprender los efectos antiinflamatorios del ejercicio podría proporcionar nuevos objetivos terapéuticos para combatir estas tendencias.
El Microbioma.
El microbioma intestinal se reconoce cada vez más como un posible contribuyente a los efectos del ejercicio, incluyendo los efectos sobre la inflamación y el metabolismo.
En un trabajo reciente del laboratorio de Xiao, los antibióticos abolieron los efectos protectores de correr en ratones después de un infarto de miocardio, y la transferencia de microbiota fecal (FMT) de ratones que hicieron ejercicio después de un infarto de miocardio atenuó la remodelación cardíaca postinfarto y mejoró la función cardíaca.
Se informó que el ejercicio aumentaba la diversidad microbiana, enriquecía géneros bacterianos beneficiosos y reducía la hipertensión en ratas espontáneamente hipertensas, indicando un papel causal del microbioma.
El microbioma también se implica en los beneficios del ejercicio para la prevención de la diabetes, un factor de riesgo cardiovascular, en humanos.
Los prediabéticos que obtuvieron beneficios glicémicos del entrenamiento con ejercicio se pudieron distinguir de aquellos que no lo hicieron basándose en cambios en su microbioma y metabolitos asociados.
Estas observaciones sugieren que los cambios en el microbioma pueden contribuir a los beneficios cardiovasculares del ejercicio.
Posibles mecanismos de los beneficios del ejercicio mediados por el microbioma.
Los efectos del ejercicio probablemente reflejen cambios en la diversidad, composición y metabolitos del microbioma.
El ejercicio regular alteró el microbioma intestinal en animales y humanos, con efectos en los filos microbianos más prevalentes en el intestino, Bacteroidetes y Firmicutes, aunque no ha surgido un patrón consistente a nivel de género.
Algunos informes sugieren que la actividad física aumenta la diversidad del microbioma intestinal, aunque no todos los estudios respaldan esta observación.
Aunque pocos estudios han abordado directamente los mecanismos por los cuales el microbioma media en los efectos del ejercicio sobre el corazón, algunos metabolitos asociados al microbioma que son modulados por el entrenamiento también afectan a fenotipos de enfermedades cardiovasculares.
Los ácidos grasos de cadena corta (SCFAs) fecales aumentan en los atletas, y los SCFAs están asociados con diversos roles, a menudo protectores, en enfermedades cardiovasculares, como la aterosclerosis, la hipertensión y la insuficiencia cardíaca.
La evidencia que respalda a los SCFAs como un vínculo entre el ejercicio, el microbioma y el riesgo cardiovascular proviene de la observación de que la resistencia a la insulina en ratones obesos mejoró con la transferencia de microbiota fecal de los respondedores al ejercicio prediabético, pero no de los no respondedores, y la suplementación de SCFAs restauró parcialmente los efectos beneficiosos en ratones trasplantados con microbiota de “no respondedores”.
En contraste, la suplementación con aminoácidos de cadena ramificada disminuyó los efectos beneficiosos en ratones trasplantados con microbiota de “respondedores”.
Finalmente, los efectos en la permeabilidad intestinal también pueden contribuir a los beneficios cardiovasculares del ejercicio.
La mucosa intestinal actúa como una barrera selectivamente permeable para la absorción de nutrientes y previene la entrada de patógenos que podrían aumentar la inflamación sistémica, un factor que impulsa las enfermedades cardiovasculares.
Mientras que el ejercicio intenso y agudo aumenta las medidas de permeabilidad intestinal en los humanos, el ejercicio crónico aumentó la integridad intestinal y la función de barrera selectiva, posiblemente a través de cambios en el microbioma intestinal.

Sarcopenia y Entrenamiento de Fuerza
Llévate esta formación, Sarcopenia y Entrenamiento de Fuerza , junto a +50 cursos de fisiología del ejercicio (fuerza, nutrición deportiva, entrenamiento, rendimiento, salud y deporte, etc...), supervisados por el Dr. Jose López Chicharro
Ejercicio y Envejecimiento.
La edad avanzada es uno de los factores de riesgo más importantes para las enfermedades cardiovasculares en general y la insuficiencia cardíaca en particular, aunque cómo contribuye exactamente el envejecimiento al desarrollo de enfermedades cardiovasculares y si es posible intervenir en este proceso siguen sin estar claros.
Los mismos procesos que impulsan el envejecimiento del organismo ocurren dentro del corazón en sí, por lo que el envejecimiento representa tanto un contribuyente sistémico como intrínseco a las enfermedades cardíacas.
Curiosamente, el ejercicio contrarresta muchas de estas vías de envejecimiento.
Consistente con este marco conceptual, el ejercicio es una de las pocas intervenciones que parece ser eficaz en la reducción del deterioro funcional cardíaco relacionado con la edad.
Por otro lado, en general, los animales de edad avanzada hacen ejercicio a intensidades más bajas que los animales jóvenes, lo que reduce el potencial de beneficios del ejercicio.
Con la edad avanzada, los corazones se hipertrofian con un aumento en el tamaño de los cardiomiocitos. Sin embargo, el efecto del ejercicio en la hipertrofia cardíaca relacionada con la edad es controvertido.
Mientras tanto, aquellos que puedan deben incorporar la actividad física en su vida diaria siempre que sea posible como una vía para prevenir y mitigar enfermedades y mejorar la calidad de vida.